引言 近期東南亞醫療器械注冊熱度持續攀升,前幾天我們在“金飛鷹藥械技術谘詢集團”公眾號陸續分享了馬來西亞和印度尼西亞注冊的相關內容,得到了粉絲朋友們的廣泛關注,本期文章繼續聚焦越南醫療器械市場,幫大家簡單梳理一下越南醫療器械注冊的關鍵流程及相關注意事項。
PART 01 法規框架
越南醫療器械監管機構為Department of Medical Equipment and Construction(DMEC) under Ministry of Health(MoH)衛生部所屬的醫療設備和建設部,其主要職責是:負責審核、批準醫療器械的注冊和監管,確保醫療器械在越南市場上符合安全性和有效性要求。
越南醫療器械注冊涉及到的主要法規有Decree No. 98/2021/ND-CPND-CP Decree on management of medical equipment《醫療器械監管法令(2021年第98號)》及Decree No.07/2023/ND-CPA mending and supplementing a number of article of Decree No. 98/2021《對2021年98號醫療器械監管法的補充法令(2023年第7號)》等。
PART 02 分類規則
越南的分類規則與馬來西亞及印尼類似,遵循 GHTF 醫療器械分類指南,根據風險由低到高,將醫療器械產品分為 A、B、C、D 四個等級(體外診斷試劑也一樣),越南衛生部在2022年發布的有關醫療器械監管法令實施細則裏明確了醫療器械的16條分類規則及體外診斷醫療器械的7條分類規則。
PART 03 產品準入路徑
在越南,A類和B類器械需獲得適用標準通知,C類和D類器械需獲得流通注冊證書(產品許可證),越南境外企業需指定當地授權代表進行相關操作。
針對A類和B類器械,越南當地授權代表需提交Declaration of Applied Standards application(適用標準的聲明)到授權代表所在的省級衛生局,以獲取營銷授權碼Marketing Authorization Code(MAC)。得到批準後,衛生局將發布適用標準通知,該通知具有終身有效性。
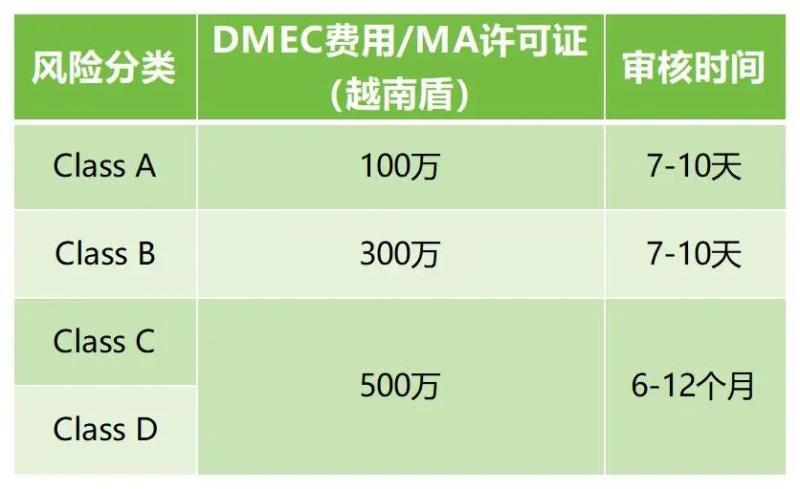
C類和D類器械在越南進口和銷售之前需要獲得市場授權(MA)許可證;當地授權代表需要提交上市注冊文檔Marketing Authorization Registration到衛生部DMEC,審核和批準後獲得永久有效的《流通注冊證》(產品許可證)。大致費用及周期如下:
PART 04 有關快速審查
在越南申請醫療器械注冊,是有快速審查路徑的。已獲得下列組織或國家之一的自由銷售證書或上市認證,在越南可適用快速審查流程:
美國食品藥品監督管理局FDA
澳大利亞藥品管理局TGA
加拿大衛生部HC
日本厚生勞動省MHLW或日本藥品醫療器械管理PMDA
歐盟(EU)
英國MHRA
中國國家藥品監督管理局NMPA
韓國食品藥品安全管理部MFDS
' fill='%23FFFFFF'%3E%3Crect x='249' y='126' width='1' height='1'%3E%3C/rect%3E%3C/g%3E%3C/g%3E%3C/svg%3E)
以上就是我們本期分享的有關越南注冊相關內容,接下來還會繼續東南亞醫療器械注冊專題分享,記得持續關注哦~假如您有東南亞注冊相關需求,歡迎隨時致電谘詢400-888-7587!
當然,假如您有其他國內外醫療器械注冊認證需求,也歡迎隨時谘詢!我們的業務範圍包括但不限於:國內外醫療器械(包含有源、無源、植入、無菌、義齒、IVD)注冊、進口醫療器械注冊、許可備案、2022世界杯欧洲区赛程时间表
、企業培訓等,國內外醫療器械注冊一站式服務,請認準金飛鷹!
越南醫療器械監管機構為Department of Medical Equipment and Construction(DMEC) under Ministry of Health(MoH)衛生部所屬的醫療設備和建設部,其主要職責是:負責審核、批準醫療器械的注冊和監管,確保醫療器械在越南市場上符合安全性和有效性要求。
越南醫療器械注冊涉及到的主要法規有Decree No. 98/2021/ND-CPND-CP Decree on management of medical equipment《醫療器械監管法令(2021年第98號)》及Decree No.07/2023/ND-CPA mending and supplementing a number of article of Decree No. 98/2021《對2021年98號醫療器械監管法的補充法令(2023年第7號)》等。
越南的分類規則與馬來西亞及印尼類似,遵循 GHTF 醫療器械分類指南,根據風險由低到高,將醫療器械產品分為 A、B、C、D 四個等級(體外診斷試劑也一樣),越南衛生部在2022年發布的有關醫療器械監管法令實施細則裏明確了醫療器械的16條分類規則及體外診斷醫療器械的7條分類規則。
在越南,A類和B類器械需獲得適用標準通知,C類和D類器械需獲得流通注冊證書(產品許可證),越南境外企業需指定當地授權代表進行相關操作。
針對A類和B類器械,越南當地授權代表需提交Declaration of Applied Standards application(適用標準的聲明)到授權代表所在的省級衛生局,以獲取營銷授權碼Marketing Authorization Code(MAC)。得到批準後,衛生局將發布適用標準通知,該通知具有終身有效性。
C類和D類器械在越南進口和銷售之前需要獲得市場授權(MA)許可證;當地授權代表需要提交上市注冊文檔Marketing Authorization Registration到衛生部DMEC,審核和批準後獲得永久有效的《流通注冊證》(產品許可證)。大致費用及周期如下:

在越南申請醫療器械注冊,是有快速審查路徑的。已獲得下列組織或國家之一的自由銷售證書或上市認證,在越南可適用快速審查流程:
美國食品藥品監督管理局FDA
澳大利亞藥品管理局TGA
加拿大衛生部HC
日本厚生勞動省MHLW或日本藥品醫療器械管理PMDA
歐盟(EU)
英國MHRA
中國國家藥品監督管理局NMPA
韓國食品藥品安全管理部MFDS
以上就是我們本期分享的有關越南注冊相關內容,接下來還會繼續東南亞醫療器械注冊專題分享,記得持續關注哦~假如您有東南亞注冊相關需求,歡迎隨時致電谘詢400-888-7587!
當然,假如您有其他國內外醫療器械注冊認證需求,也歡迎隨時谘詢!我們的業務範圍包括但不限於:國內外醫療器械(包含有源、無源、植入、無菌、義齒、IVD)注冊、進口醫療器械注冊、許可備案、2022世界杯欧洲区赛程时间表 、企業培訓等,國內外醫療器械注冊一站式服務,請認準金飛鷹!
' fill='%23FFFFFF'%3E%3Crect x='249' y='126' width='1' height='1'%3E%3C/rect%3E%3C/g%3E%3C/g%3E%3C/svg%3E)
金飛鷹介紹
金飛鷹是國內領先的醫療器械一站式注冊認證谘詢與軟件開發管理綜合性服務集團公司,成立於2007年。集團總部位於深圳南山,並先後在廣州、四川、湖南、江蘇、廣西、湖北、重慶等多地設立分支機構及辦事處。
集團以“誠信、務實、專業、專注”的服務理念,為國內&國外醫療器械研發者、生產者、經營者、使用者提供從產品立項、設計開發、廠房選址、廠房平麵布局規劃、潔淨廠房設計規劃、企業硬件配置、設備選型、配置到人力資源組建、產品技術要求製定、檢驗檢測輔導跟蹤、臨床評價、臨床試驗、質量管理體係(GMP、GSP、GB/T 42061、ISO 13485、QSR 820、MDSAP多國認證等)建立、運行、審核、獲證的“全方位、一站式”醫療器械產業專業解決方案。
金飛鷹在美容類醫療器械產品領域積累了豐富的國內外注冊/認證輔導經驗,主要包括有源產品中的激光、強脈衝光(IPL、DPL、牛奶光)、紅藍紫光、RF射頻、超聲、中低頻電刺激及電子助推裝置類等;無源產品中的醫用重組型膠原蛋白、透明質酸鈉、無針注射器、液體成膜敷料類等;服務區域包括國內注冊/進口注冊,美國FDA、歐盟CE認證、英國UKCA、加拿大MDL/MDEL、澳大利亞、巴西、沙特、日本、韓國、東南亞等國外注冊。,時02:07
金飛鷹是國內領先的醫療器械一站式注冊認證谘詢與軟件開發管理綜合性服務集團公司,成立於2007年。集團總部位於深圳南山,並先後在廣州、四川、湖南、江蘇、廣西、湖北、重慶等多地設立分支機構及辦事處。
集團以“誠信、務實、專業、專注”的服務理念,為國內&國外醫療器械研發者、生產者、經營者、使用者提供從產品立項、設計開發、廠房選址、廠房平麵布局規劃、潔淨廠房設計規劃、企業硬件配置、設備選型、配置到人力資源組建、產品技術要求製定、檢驗檢測輔導跟蹤、臨床評價、臨床試驗、質量管理體係(GMP、GSP、GB/T 42061、ISO 13485、QSR 820、MDSAP多國認證等)建立、運行、審核、獲證的“全方位、一站式”醫療器械產業專業解決方案。
金飛鷹在美容類醫療器械產品領域積累了豐富的國內外注冊/認證輔導經驗,主要包括有源產品中的激光、強脈衝光(IPL、DPL、牛奶光)、紅藍紫光、RF射頻、超聲、中低頻電刺激及電子助推裝置類等;無源產品中的醫用重組型膠原蛋白、透明質酸鈉、無針注射器、液體成膜敷料類等;服務區域包括國內注冊/進口注冊,美國FDA、歐盟CE認證、英國UKCA、加拿大MDL/MDEL、澳大利亞、巴西、沙特、日本、韓國、東南亞等國外注冊。,時02:07
醫療器械注冊谘詢認準金飛鷹
深圳:0755-86194173
廣州:020 - 82177679
四川:028 - 68214295
湖南:0731-22881823
湖北:181-3873-5940
江蘇:135-5494-7827
廣西:188-2288-8311
海南:135-3810-3052
重慶:135-0283-7139


