
類風濕性關節炎(RA)是最常見、最具破壞性的係統性自身免疫疾病之一,其特點是關節免疫功能障礙,伴有嚴重的滑膜炎和不可逆的骨質破壞、軟骨侵蝕,甚至致殘。
最近的研究表明,活性氧(ROS)的無節製過量產生和缺氧微環境是導致關節免疫功能障礙和最終關節侵蝕的關鍵因素,其途徑包括氧化應激升高、破壞細胞代謝功能以至細胞凋亡,以及激活巨噬細胞的促炎表達,從而誘導炎性細胞因子的過度表達、 組織壞死因子α (TNF-α)、白細胞介素 1β (IL-1β) 和白細胞介素 6 (IL-6),從而加劇了高免疫原性炎症的複雜微環境。盡管臨床上批準的多種免疫抑製劑可以暫時緩解炎症症狀,但它們並不能解決疾病的根本原因,而且長期用藥會產生嚴重的副作用,如免疫係統功能減弱和感染風險增加。
考慮到這些問題的嚴重性,應進一步致力於開發一種具有清除 ROS 和抗炎功能的生物安全多功能幹預係統,以徹底治療 RA。間充質幹細胞(MSCs)衍生的細胞外囊泡(EVs)是一種小尺寸的磷脂雙分子層,直徑從50到1000納米不等,攜帶著宿主間充質幹細胞的蛋白質、mRNA和miRNA等生物活性分子,具有靶向聚集在炎症部位、抗凋亡和促進再生的特點。特別是,先前的研究證明,骨髓幹細胞(BMSCs)衍生的EVs(BEVs)可對炎症部位產生靶向效應,改善炎症微環境,保護軟骨細胞。 盡管 BEVs 在 RA 治療初期可通過遞送調節細胞因子抑製 M1 巨噬細胞極化並促進抗炎介質的表達,但其有限的抗 ROS 能力和體內遷移能力對維持長期療效構成了挑戰。因此,基於 BEVs 的細胞間轉運能力,複合具有高效清除 ROS 和持續供氧的多功能製劑,為長期持續重建關節免疫穩態創造適宜的微環境,對抑製 RA 的進展具有重要意義。
縱觀生物機體,已進化出一套精確的抗氧化防禦係統來抵消 ROS 對機體的有害影響,該係統主要由過氧化氫酶(CAT)和超氧化物歧化酶(SOD)等抗氧化酶組成,這些酶與供氫底物或輔酶共同促進質子和電子的快速轉移過程,從而有效中和超氧陰離子(-O2-)和過氧化氫(H2O2),維持體內平衡。 然而,基於抗氧化物酶的療法也表現出一些固有的缺點,如循環半衰期短、細胞滲透性低和抗原性,這限製了其在治療炎症損傷部位的直接應用。
一種潛在的策略是通過模仿天然抗氧化酶迅速的質子和電子轉移機製,創造出具有多種催化活性的人工生物催化材料,用於各種抗氧化治療目的。 在各種生物催化材料(如金屬納米顆粒、基於納米碳或聚合物的酶模擬物)中,基於金屬氧化物的生物催化劑因其良好的生物相容性、結構多樣性、可行的改性、可調的催化位點和成本效益而受到廣泛關注。
然而,目前基於金屬氧化物的 ROS 生物催化劑在複雜的炎症微環境中的應用仍麵臨一些挑戰:1) 純金屬氧化物材料的生物催化活性極低,ROS 清除類型有限,缺乏智能和生物適應性催化特性,通常需要大劑量的藥劑幹預,不可避免地會引發細胞毒性和其他附帶副作用;2) 金屬氧化物表麵構建的額外催化位點通常因廣泛的金屬氧配位而呈現較高的氧化態,這有助於在 ROS 催化過程中與氧物種牢固結合,最終降低整體反應速率。因此,當務之急是開發有效的管理策略來調節金屬氧化物支持的催化位點的微環境,從而衍生出多功能、高效和穩健的人工抗氧化劑,以滿足 RA 治療的複雜需求。
基於背景提及的問題,四川大學程衝教授、四川大學華西醫院邱邐教授等人合成了生物催化和氧化還原調控納米結構,用於精確調節炎症和免疫平衡以防治類風濕性關節炎。相關成就Biocatalytic and Redox-Regulated Nanoarchitectures for Precision Inflammation and Immune Homeostasis Modulation to Combat Rheumatoid Arthritis為題發表在 Advanced Materials。我們將該文獻部分內容轉載如下,以供相關企業學習參考。
在這裏,設計了一種新的生物催化和氧化還原調控納米結構--塗有 BEVs 的 Ru 簇錨定羥基化 Fe2O3(Ru-HFO),用於精確調節炎症,以防治 RA。當與超聲波(US)刺激相結合時,這種生物催化和炎症靶向納米結構(BEVs@Ru-HFO)可對巨噬細胞和破骨細胞進行重編程,以控製氧化還原和免疫平衡,從而緩解 RA(圖 1)。
這項工作的主要動機來自兩個概念:1)獨特的羥基化策略提高了 Ru 氧化還原中心的電子密度,優化了氧中間產物的結合強度,確保了卓越的抗氧化酶催化 ROS 消除活性;2)應用 US 和封裝 BEVs 可以促進 HFO 在炎症部位的精確靶向、遞送和聚集,從而顯著放大治療效果。值得注意的是,我們的實驗研究和理論分析表明,羥基化結構能顯著調節 HFO 底物與 Ru 氧化還原中心之間的電子相互作用,引發具有高電子密度態的 Ru 團簇位點的形成;此外,羥基還能作為 H 供體推動質子快速轉移,從而協同加快反應速度。
因此,Ru-HFO 同時具有出色的-OH 清除、SOD 和 CAT 模擬活性,可消除 ROS,並具有持續穩定的氧合能力。在 US 的輔助下,BEVs@Ru-HFO 可減輕 M1 巨噬細胞的氧化應激,促進其向抗炎 M2 表型的再極化,並逆轉缺氧環境,抑製破骨細胞的生成過程,最終達到保護軟骨和恢複關節功能的效果。引人注目的是,這種生物啟發的生物催化和氧化還原調控納米結構在關節炎症緩解過程中顯示出卓越的體內氧化還原和免疫平衡調節能力,這為設計新型抗氧化酶樣材料提供了一條前景廣闊的途徑,有望解決各種炎症性疾病。
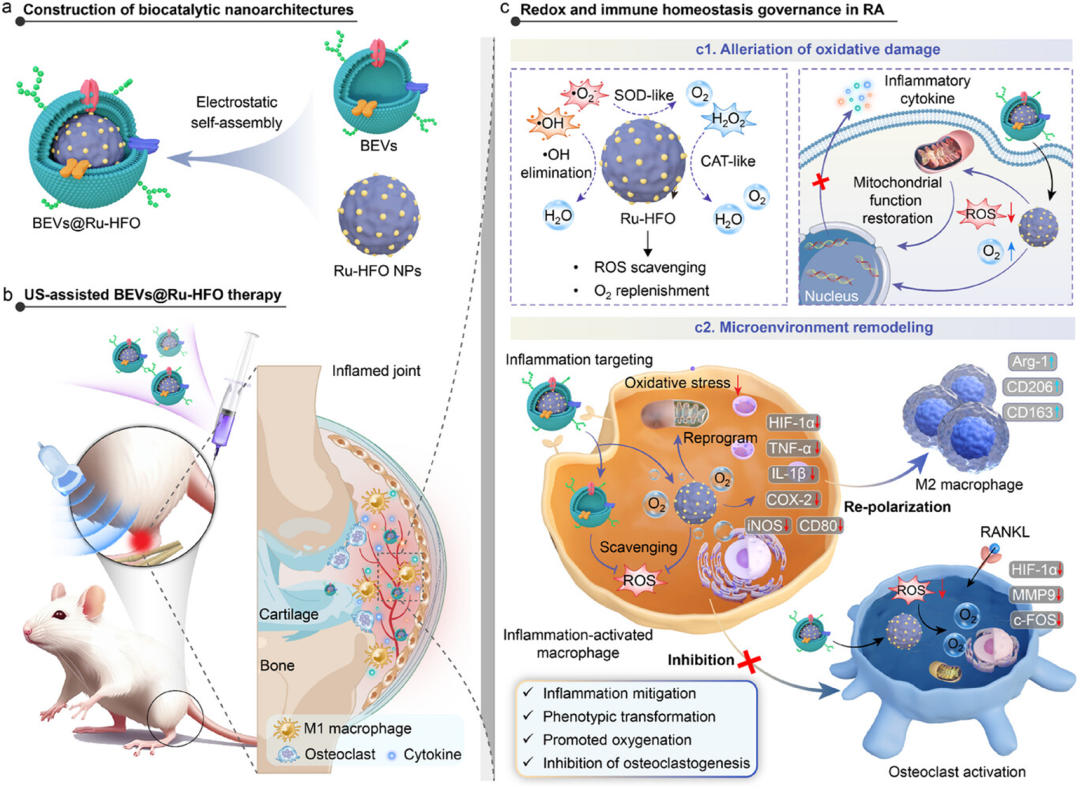
圖 1. 綜述BEVs@Ru-HFO調節氧化還原和免疫穩態以緩解RA的機製。a) 通過靜電自組裝構建生物催化和氧化還原調控納米結構(BEVs@Ru-HFO)。b) BEVs@Ru-HFO 在美國協助下靶向炎症部位的圖解。 c) 氧化還原和免疫平衡在 RA 中的卓越重塑特性,它整合了缺氧緩解和 ROS 清除功能,可調節巨噬細胞表型,抑製破骨細胞生成,並最終逆轉骨侵蝕。
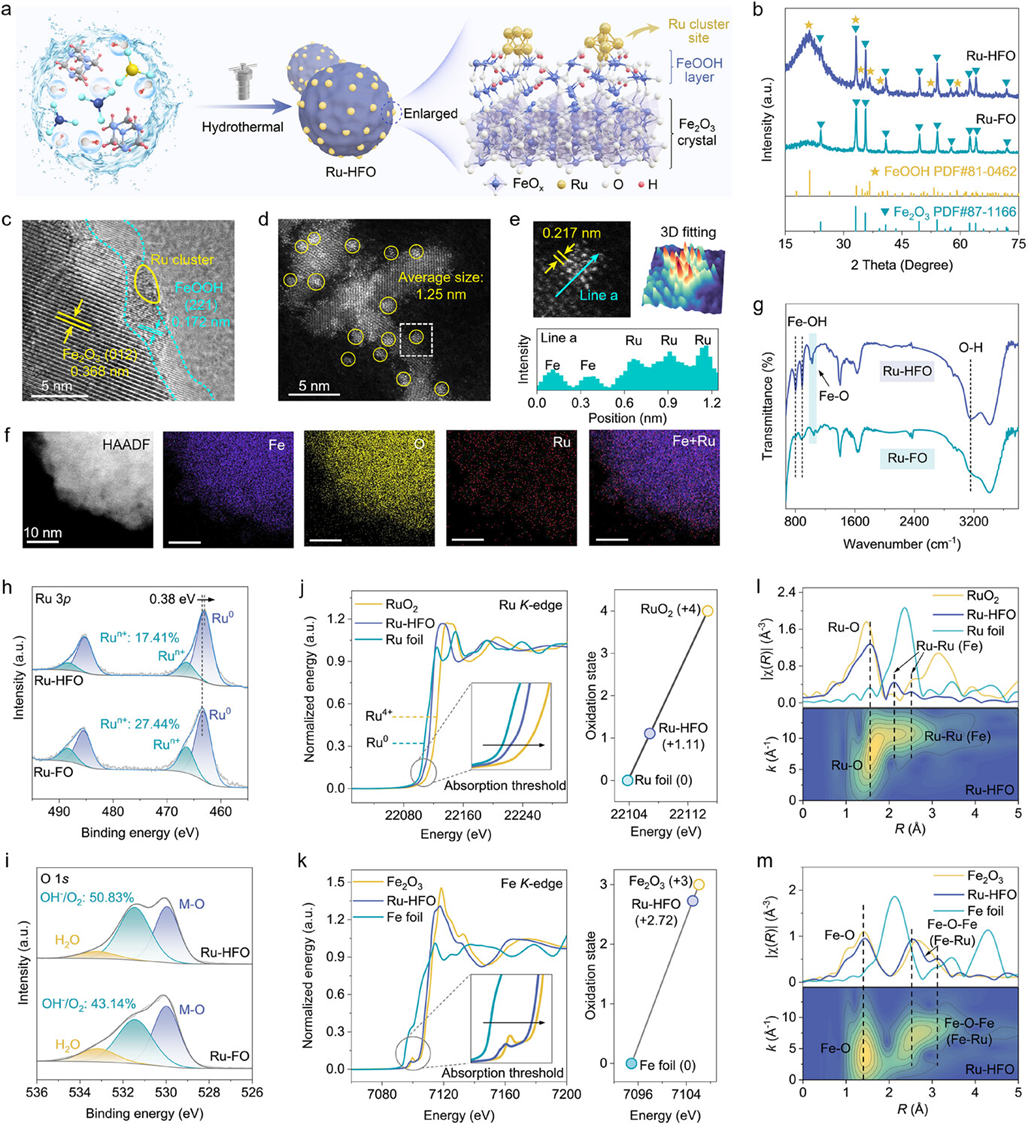
圖 2. Ru-HFO的製備及結構表征。a) Ru-HFO 的製造過程示意圖。 b) Ru-HFO 和 Ru-FO 的 XRD 圖譜。 c) Ru-HFO 的 HR-TEM 圖像。j) Ru K 邊的 XANES 光譜,以及根據 XANES 的差異計算出的相應 Ru 價態; k) Fe K 邊的 XANES 光譜,以及根據 XANES 的差異計算出的相應 Fe 價態。l) Ru-HFO 和參考物的傅立葉變換 EXAFS k2 加權 χ(k)函數譜圖以及 Ru-HFO 的 WT 分析。 m) Ru-HFO 和參考物的傅立葉變換 EXAFS k2 加權 χ(k)函數譜圖以及 Ru-HFO 的 WT 分析。
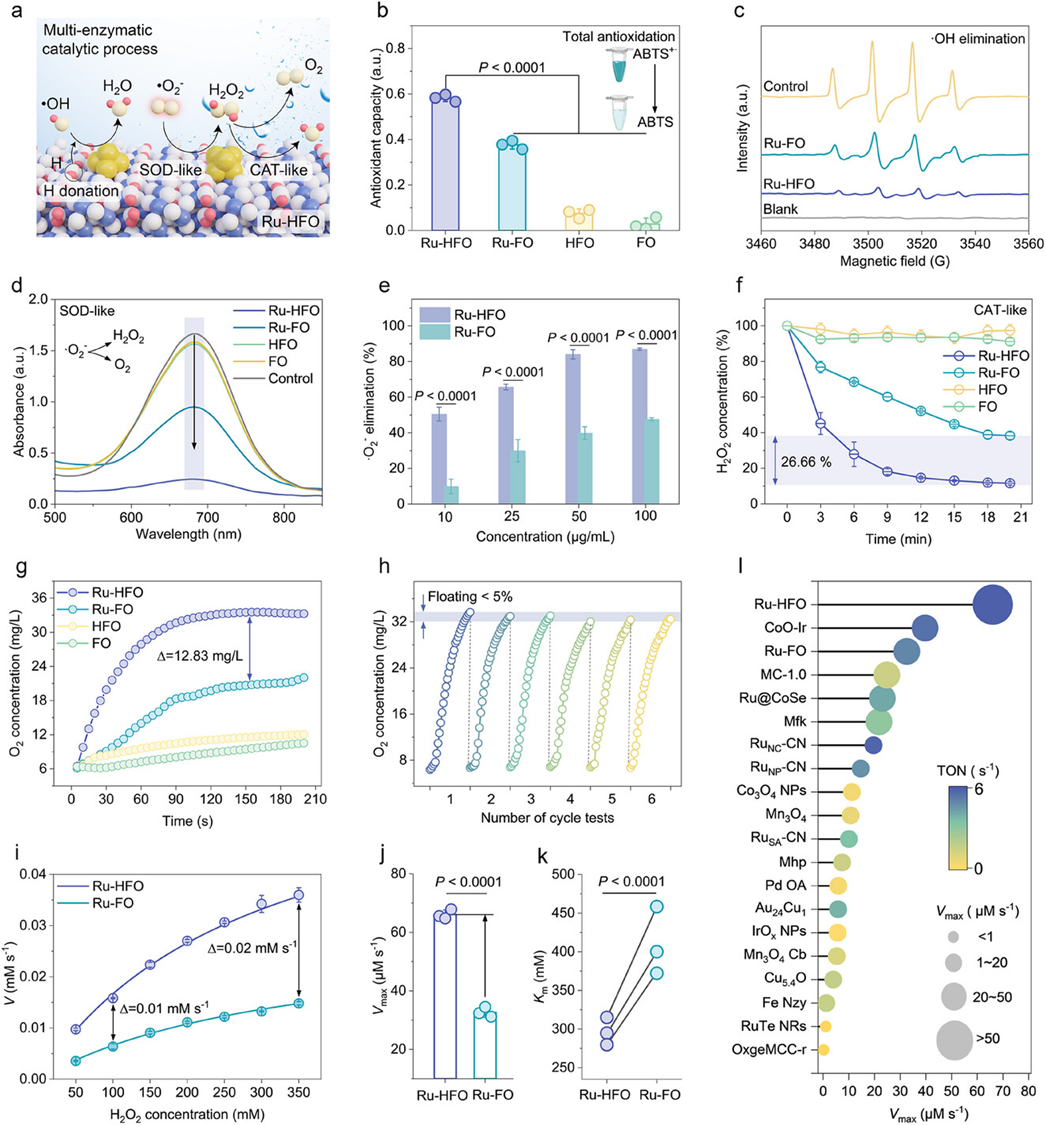
圖 3. 多酶活性氧清除活性的評價。a) 類多酶催化反應的示意圖,包括 -OH 消除、類 SOD 和類 CAT 反應。 b) 通過 ABTS+- 還原比較不同生物催化劑的抗氧化能力(n = 3 個獨立實驗,數據以均值 ± S.D. 表示)。e) Ru-HFO 和 Ru-FO 在不同濃度下的 SOD 樣活性(n = 3 次獨立實驗,數據以均值 ± S.D. 表示)。 f) 通過基於 TiSO4 的方法,在生物催化劑和 H2O2 存在的情況下,CAT 樣性能隨時間變化(n = 3 次獨立實驗,數據以均值 ± S.D. 表示)。g)在存在生物催化劑和H2O2的情況下,用氧氣溶解儀測量產生的O2濃度。h) Ru-HFO 產生 O2 的穩定性測試。 i) 以 H2O2 為底物的 Ru-HFO 和 Ru-FO 的 Michaelis-Menten 動力學分析(n = 3 個獨立實驗,數據以均數 ± S.D. 表示)。j) Ru-HFO 和 Ru-FO 的 Vmax 值(n = 3 次獨立實驗,數據以均值 ± S.D. 表示)。 k) Ru-HFO 和 Ru-FO 的 Km 值(n = 3 次獨立實驗,數據以均值 ± S.D. 表示)。 l) 與之前發表的最先進的酶模擬材料的 TON 值和 Vmax 值的比較和分析。b) 中 P 值的評估是通過雙尾單向方差分析(ANOVA)和 Tukey 後檢驗進行多重比較。a.u.表示任意單位。
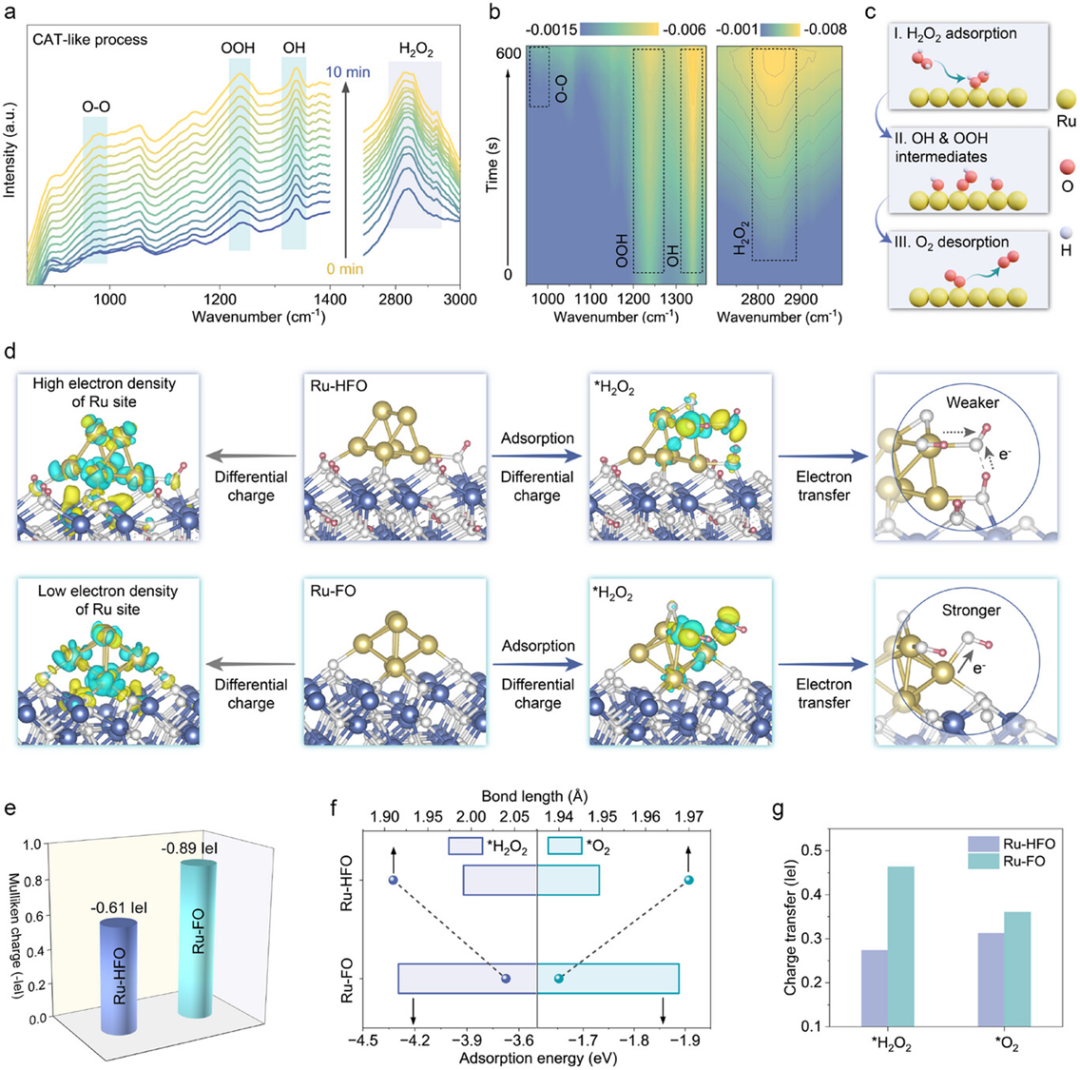
圖 4. a, b) Ru-HFO 類 CAT 反應過程的原位傅立葉變換紅外光譜隨時間變化的測試。 c) Ru-HFO 誘導類 CAT 反應的示意過程。 d) Ru 位點的差電荷密度分析、H2O2 在 Ru-HFO 和 Ru-FO 上的吸附情況以及配位環境中的電子流。黃色和青色等值麵分別表示電子密度的積累和耗盡。 e) Ru-HFO 和 Ru-FO 中 Ru 位點的穆利肯電荷分析。 f) Ru-HFO 和 Ru-FO 與 *H2O2 和 *O2 作用時的鍵長和吸附能。
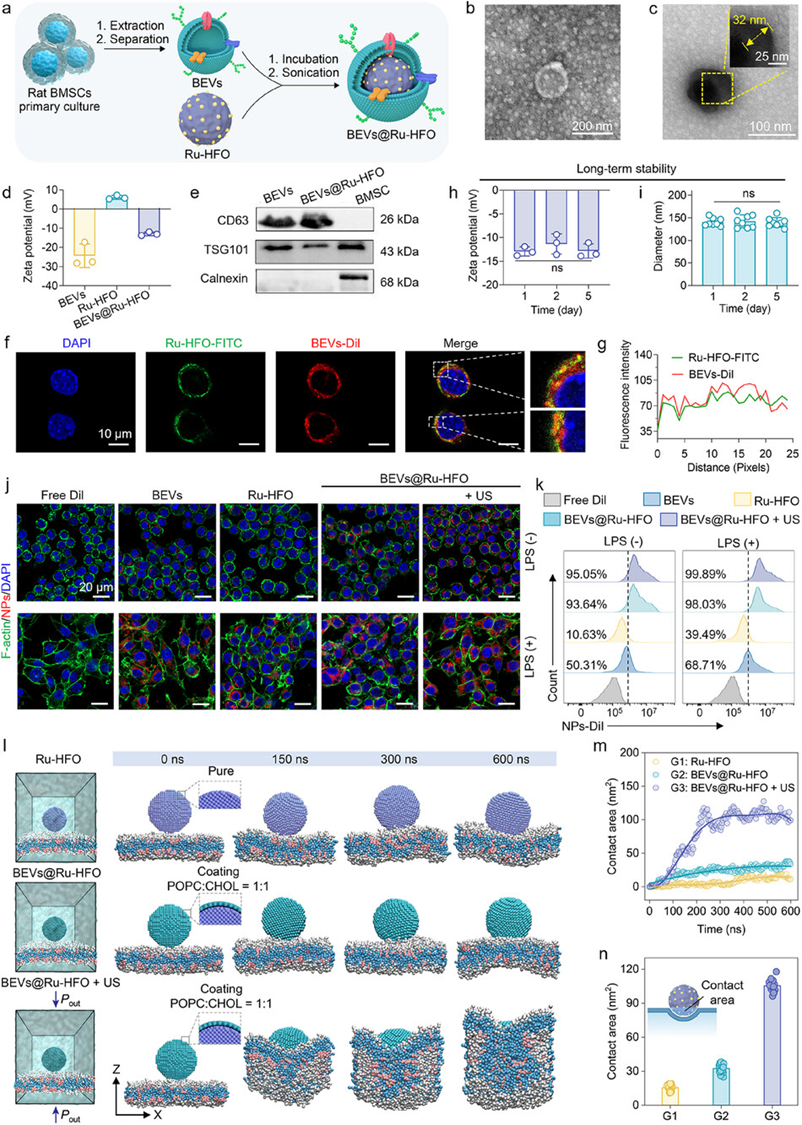
圖 5. a) BEVs-encapsulated Ru-HFO 生物催化劑的製備過程示意圖。d) BEVs、Ru-HFO NPs 和 BEVs@Ru-HFO 的 Zeta 電位(n = 3 次獨立實驗,數據以均值 ± S.D. 表示)。e) Western 印跡分析 BMSCs、BEVs 或 BEVs@Ru-HFO NPs 表達的 BEVs 標記(CD63、TSG101)和 calnexin。藍色熒光表示用 4′,6-二脒基-2-苯基吲哚(DAPI)標記的 RAW 264.7 細胞核。g) 用於共定位分析的熒光強度曲線。從(h)zeta 電位值(n = 3 次獨立實驗,數據以均值 ± S.D. 表示)和(i)流體力學直徑(n = 8 次獨立實驗,數據以均值 ± S.D. 表示)分析 BEVs@Ru-HFO 的長期穩定性。j) 未激活和 LPS 激活的 RAW 264.7 巨噬細胞攝取 Dil 標記材料的代表性 CLSM 圖像。細胞骨架和細胞核分別用 Alexa Fluor 488(綠色)和 DAPI(藍色)標記。比例尺:20 微米。) l) 磷脂雙分子層上純 Ru-HFO、BEVs@Ru-HFO 和 US 相互作用的 BEVs@Ru-HFO 納米粒子的代表性分子動力學模擬快照。m) 不同處理組的納米粒子與磷脂雙分子層的接觸麵積沿膜法線位置的時間演變。 n) 不同處理組在最終平衡位置的接觸麵積比較(n = 15,數據以均值 ± S.D. 表示)。b、c、e、f、j、k)中的圖像是三次獨立重複實驗的結果。P 值通過雙尾單因素方差分析和 Tukey 後檢驗進行多重比較。

圖 6. a) RAW 264.7(正常組)或缺氧條件下 LPS 激活的 RAW 264.7 處理前(LH 組)或 Ru-HFO 處理後(LH + Ru-HFO 組)基因的 PCA。b) 正常組、LH 組和 LH + Ru-HFO 組基因的 Violin 圖。(d) KEGG 富集分析和 (e) GO 富集分析中 RAW 264.7 經 Ru-HFO 處理後的調節途徑和過程。 f) ROS 清除和缺氧抑製的可能體外機製示意圖。比例尺:100 µm: h) DCFH-DA 的熒光強度定量(n = 3 個獨立的生物重複)。 i) HIF-1α 的熒光強度定量(n = 3 個獨立的生物重複)。 j) 在炎症(LPS)和缺氧條件下培養並接受不同處理的 RAW 264.7 中 HIF-1α 的蛋白表達,通過 Western 印跡分析進行評估。. g、j)中的圖像是三次獨立重複實驗的結果。數據以均數 ± S.D 表示。P 值的評估采用雙尾單因素方差分析,並用 Tukey 後檢驗進行多重比較。星號表示差異顯著,*p < 0.05,****p < 0.0001,ns 表示不顯著。a.u. 表示任意單位。
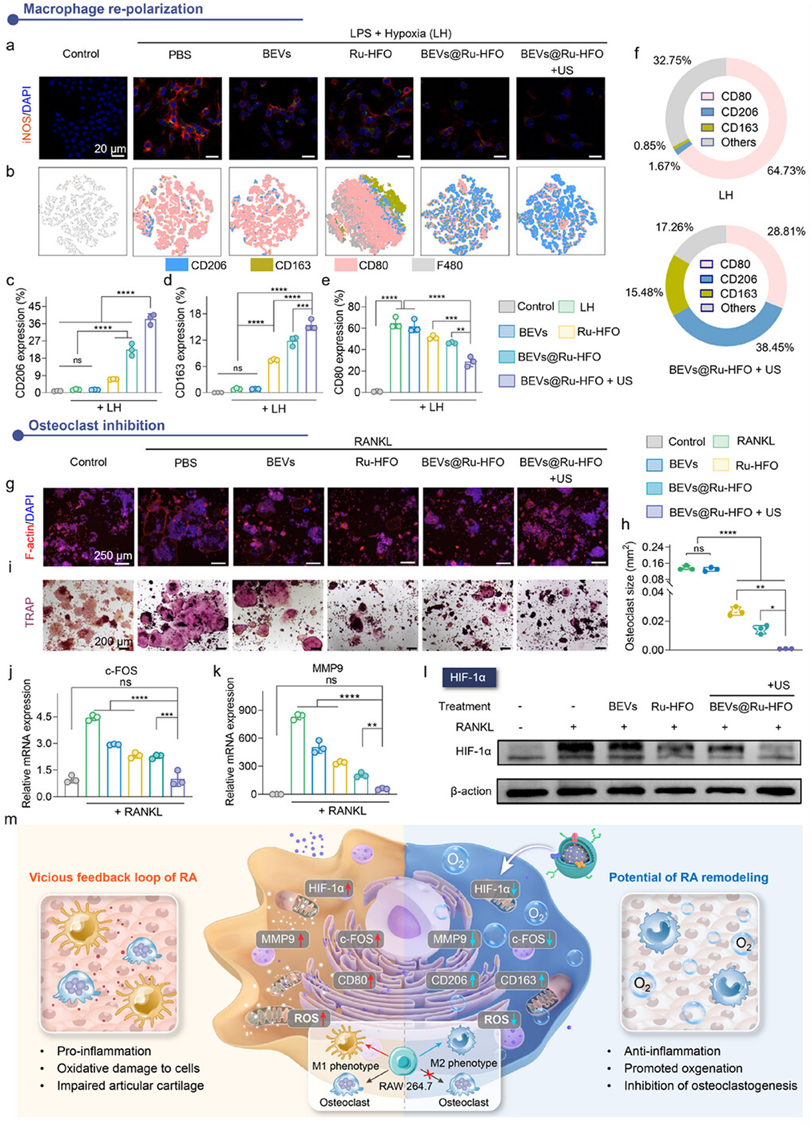
圖 7.巨噬細胞複極化與破骨細胞生成的抑製。a) 不同處理後 RAW 264.7 的 iNOS(紅色)和 DAPI(藍色)染色的 CLSM 圖像,分別顯示 M1 巨噬細胞標記和細胞核的可視化。b) 不同處理後 RAW 264.7 的 CD80、CD206 和 CD163 的 FCM 分析。f) LH 組和 BEVs@Ru-HFO + US 組中 CD80、CD206 和 CD163 表達水平比例的環形圖(n = 3 個獨立生物重複)。 g) 肌動蛋白環形成實驗中羅丹明類黃酮(紅色)染色圖像,細胞核用 DAPI(藍色)染色。h) 破骨細胞大小的統計分析(n = 3 個獨立生物重複)。 i) 不同處理組的代表性 TRAP 染色圖像。比例尺:200 µm。l) 不同處理後 RANKL 刺激的 RAW 264.7 中 HIF-1α 蛋白表達水平的 Western 印跡分析。 m) 不同處理抑製巨噬細胞再極化和破骨細胞形成的可能細胞機製示意圖。a、b、g、i、l)中的圖像是三次獨立重複實驗的結果。數據以均數 ± S.D 表示。P 值的評估采用雙尾單因素方差分析,並進行 Tukey 後檢驗進行多重比較。星號表示差異顯著,*p < 0.05,**p < 0.01,***p < 0.001,****p < 0.0001,ns 表示不顯著。
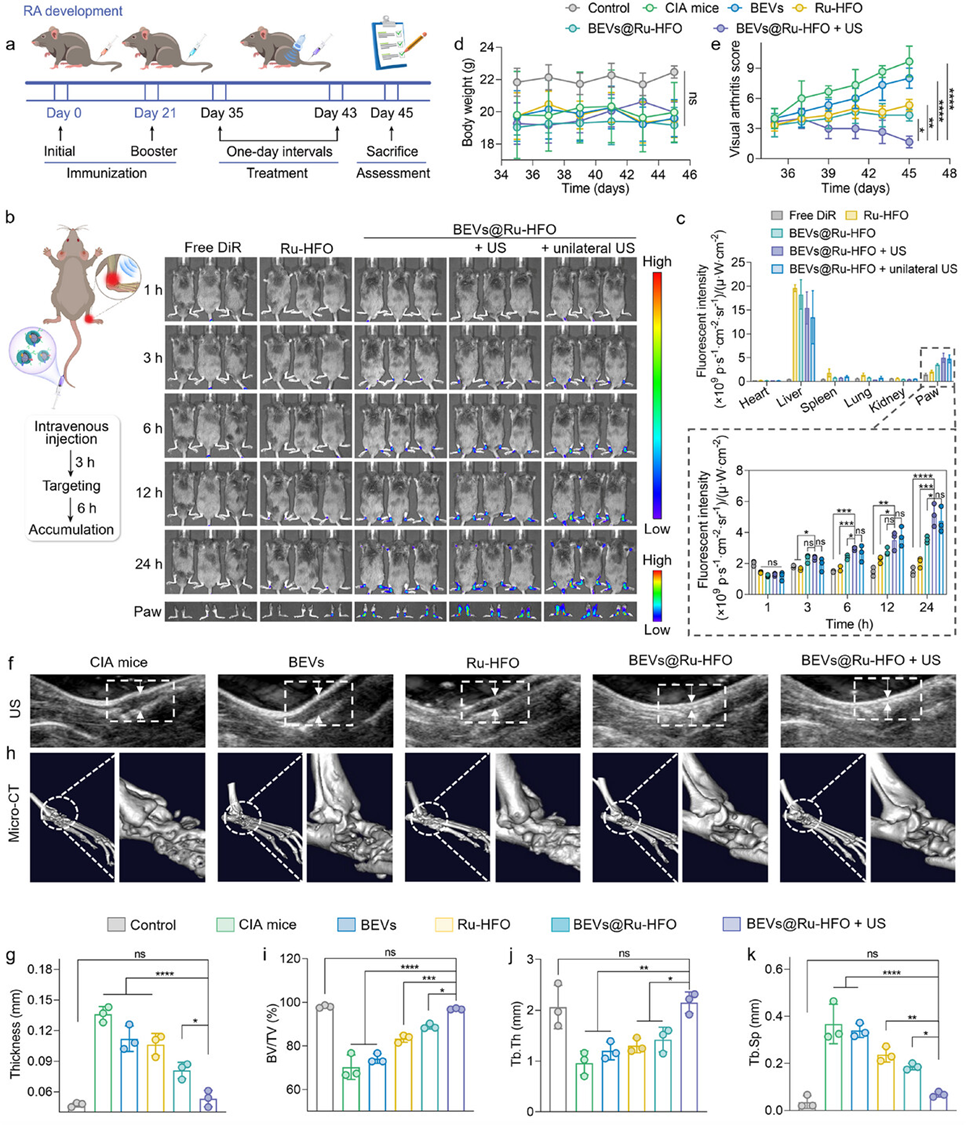
圖 8. BEVs@Ru-HFO在RA模型中的生物分布及治療效果。a) CIA 小鼠模型的治療方案。b) 小鼠靜脈注射遊離的 1,1′-二辛基-3,3,3′,3′-四甲基碘化吲哚(DiR)、DiR 標記的 Ru-HFO、BEVs@Ru-HFO、BEVs@Ru-HFO + US 和 BEVs@Ru-HFO + 單側 US 後,在不同時間間隔捕獲的實時體內熒光成像。c) 主要器官的相應半定量分析。d) 各組小鼠在不同時間點的體重(每組 3 隻獨立生物學小鼠)。f) 不同組小鼠踝關節的代表性 US 圖像。) 通過 US 測定的關節厚度定量(n = 每組 3 隻獨立生物學小鼠)。 h) 不同組小鼠踝關節的代表性顯微 CT 掃描圖像。f、h)中的圖像是三次獨立重複實驗的代表。顯微 CT 組織形態計量參數的定量分析,包括 (i) 骨量(BV/TV);(j) 骨小梁厚度(Tb.Th);(k) 骨小梁分離度(Tb.Sp)(n = 每組 3 隻生物獨立小鼠)。數據以均數 ± S.D 表示。P 值的評估采用雙尾單向方差分析,並用 Tukey 後檢驗進行多重比較。星號表示差異顯著,*p < 0.05,**p < 0.01,***p < 0.001,****p < 0.0001,ns 表示不顯著。
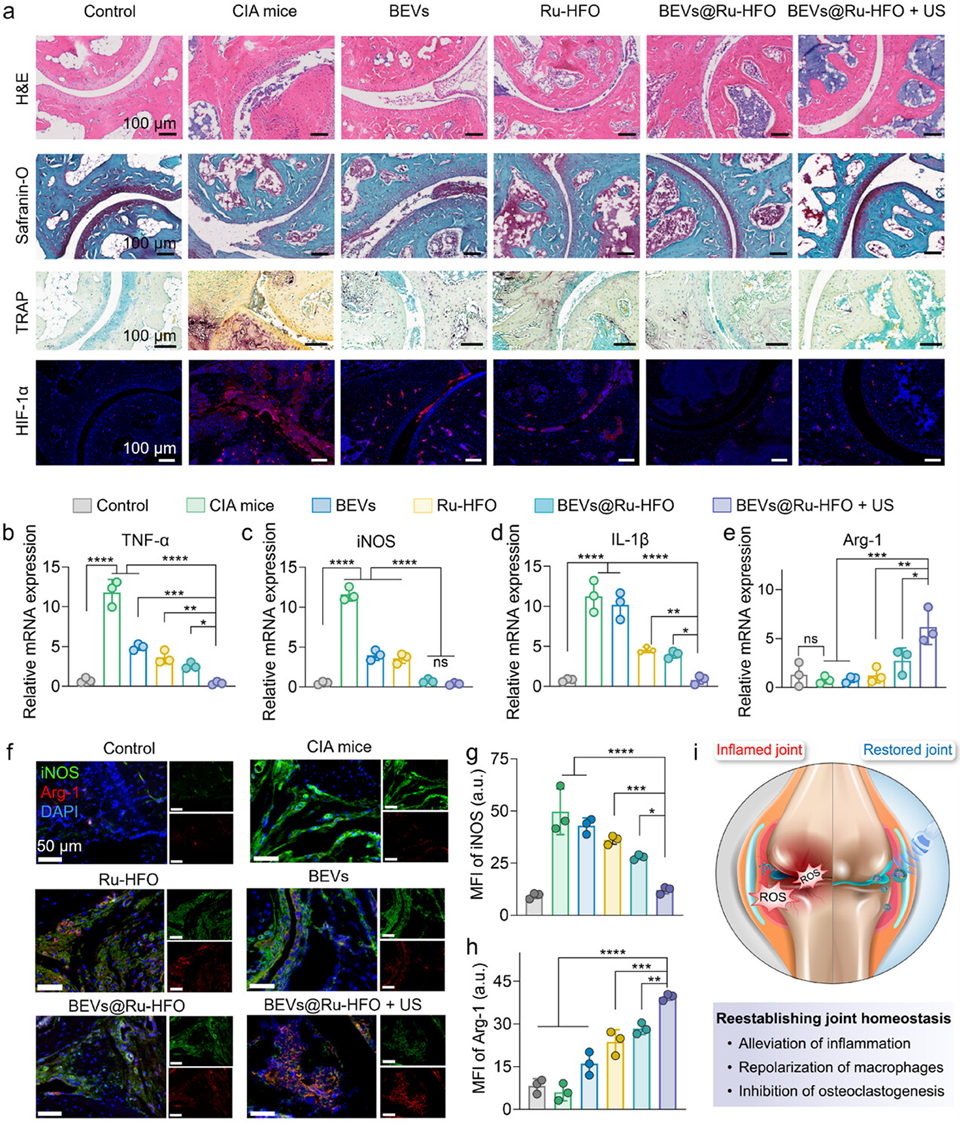
圖 9. a) 免疫組化評估,包括組織學評估,包括不同治療後 RA 關節的 H&E 染色、Safranin-O 染色、TRAP 染色和滑膜的 HIF-1α 染色(紅色)。b, c) RT-qPCR 分析接受指定治療的 CIA 小鼠滑膜中 M1(TNF-α 和 iNOS)和(d)炎性細胞因子(IL-1β)以及(e)M2(Arg-1)巨噬細胞標記物的相對 mRNA 表達水平(n = 每組 3 隻生物學上獨立的小鼠)。f) 不同治療組滑膜巨噬細胞標記物的免疫組化評估,包括 M1 標記物(iNOS,綠色)和 M2 標記物(Arg-1,紅色)染色。標尺 = 50 µm。i) 可能的治療機製示意圖。a、f)中的免疫熒光染色圖像是三次獨立重複實驗的代表。數據以均數 ± S.D 表示。P 值的評估采用雙尾單向方差分析,並對多重比較進行 Tukey 後檢驗。星號表示差異顯著,*p < 0.05,**p < 0.01,***p < 0.001,****p < 0.0001,ns 表示不顯著。a.u. 表示任意單位。
我們的創新方法解決了傳統 BEVs 的局限性,特別是其抗炎效果不理想和體內炎症部位靶向受限的問題。通過設計新型抗氧化劑生物催化劑並將其戰略性地融入 BEV,再加上超聲波介導的靶向遞送,我們開發出了一種更有效的治療平台,用於在 RA 抗氧化療法中精確調節炎症,從而顯著促進關節氧化還原和免疫平衡的重建。我們對BEVs@Ru-HFO的治療優勢進行了細致的研究,確定了以下三個組成部分:1) 卓越的多功能抗氧化酶樣活性和持續氧合能力,可提供適當的 RA 修複微環境;2) 細胞外囊泡可精確靶向炎症部位並輔助免疫調節;3) US 輔助細胞攝取和主動靶向 RA 的能力。實驗分析和理論計算證實,合成的 Ru-HFO 生物催化劑具有創新的羥基化結構和富含電子的 Ru 位點,能促進質子和電子的快速轉移,並能有效地與氧物種發生反應,最終賦予其最佳的 ROS 清除能力。我們的轉錄分析表明,Ru-HFO 可通過調節相關基因和信號通路的表達,使炎症和氧化應激表型向變性方向轉變。同時,係統的體外研究發現,BEVs@Ru-HFO 可減輕 M1 巨噬細胞的氧化應激,促使其向抗炎 M2 表型極化,從而有效逆轉其抑製性免疫效應。此外,缺氧環境的緩解阻礙了破骨細胞的生成過程,從而有利於關節修複和骨/軟骨保護。此外,BEVs@Ru-HFO 在體內小鼠模型中表現出的顯著療效進一步證實,BEVs@Ru-HFO 不僅能通過減少炎性細胞因子的表達重塑免疫屏障,緩解關節腫脹,還能促進骨/軟骨修複。我們預計,所設計的生物催化和氧化還原調控納米結構將為治療 RA 提供一種前景廣闊的策略,並為解決與氧化應激相關的炎症性疾病開辟新的途徑。
1. 羥基化金屬簇催化機製創新:首次通過羥基化策略優化Ru-Fe₂O₃納米結構的電子密度與催化活性,羥基化使Ru氧化還原中心的d帶中心上移,提升對氧中間產物(如O₂⁻、H₂O₂)的吸附親和力,同時羥基作為質子供體加速電子轉移,使Ru-HFO兼具超氧化物歧化酶(SOD)、過氧化氫酶(CAT)和·OH清除三重酶模擬活性,ROS清除效率比非羥基化材料提升4倍。
2. 生物仿生靶向與超聲響應遞送創新:構建細菌外囊泡(BEVs)修飾的智能靶向係統,結合超聲(US)實現炎症部位精準富集,BEVs表麵的炎症靶向肽(如整合素結合序列)使納米結構在RA關節的聚集量比正常組織高5.8倍,減少全身分布毒性。
3. 氧化還原-免疫雙平衡調控創新:提出“清除ROS+極化巨噬細胞+抑製破骨細胞”三重治療策略,Ru-HFO通過降低M1型巨噬細胞內ROS水平(如·OH減少70%),上調抗炎因子IL-10表達(增加2.3倍),促進其向M2修複表型轉化,關節炎症評分降低45%。
原文鏈接:
https://doi.org/10.1016/j.biomaterials.2025.123413
聲明:本文內容僅用於學術交流與學習參考,所涉文章版權歸原作者及出版機構所有。如涉及侵權或未授權使用,請聯係本公眾號管理員,我們將立即刪除相關內容。
往期精彩推薦
醫療器械注冊谘詢認準金飛鷹
深圳:0755-86194173
廣州:020 - 82177679
四川:028 - 68214295
湖南:0731-22881823
湖北:181-3873-5940
江蘇:135-5494-7827
廣西:188-2288-8311
海南:135-3810-3052
重慶:135-0283-7139


